

染色质/卡拉胶复合材料高效吸附苯并蒽的特性与影响因素分析
(广西科技大学生物与化学工程学院, 柳州 545006)
摘要: 苯并蒽 (BaA) 是多环芳烃 (PAHs) 中最重要的污染物之一, 具有分布广泛、稳定性强、生物累积性强、致癌性强等特点, 严重危害人类健康和环境。本项研究中, 基于BaA 和DNA之间的插层结合, 我们制备了一种新型的染色质/卡拉胶复合材料, 它是一种简单有效的吸附剂, 可以有效地从水溶液中吸附BaA。在最佳条件下, 染色质/卡拉胶复合材料对BaA吸附率为94%, 吸附量为0. 0075mg·g-1, 该吸附过程受到反应时间、反应温度、pH值和复合材料剂量的影响, 其中, 高温或低温、酸性或碱性环境都会降低吸附率。然而, 随着反应时间的延长或复合材料剂量的增加, 吸附率将逐渐提高。染色质/卡拉胶复合材料去除BaA的过程更符合准二级动力学模型和Langmuir模型, 且热力学模型进一步表明该过程是自发进行的。以上结果表明, 染色质/卡拉胶复合材料可以作为吸附BaA的新型吸附剂。
引用格式: 臧萌, 李军生, 黄国霞, 等. 染色质/卡拉胶复合材料高效吸附苯并蒽的特性与影响因素分析[J]. 交叉科学学报, 2025, 2(1): 22-36.
文章类型: 研究性论文
收稿日期: 2025-02-26
接收日期: 2025-03-02
出版日期: 2025-03-28
1 引言
BaA是一种典型的四环芳烃,存在于煤焦油、沥青、杂酚油、各种燃煤烟气以及汽车发动机尾气中。由于合成洗涤剂的不当使用,导致BaA在洗涤剂的帮助下溶解在水中,并分散到不同的土壤中[1]。因此,一方面,包括中国在内的许多国家和地区的土壤中BaA的含量和检出率都很高[2,3];另一方面,由于BaA不能生物降解,它可以在食物链中传播、积累和扩散,伤害更多的生物体,最终危及整个环境和人类健康[4,5]。目前,BaA的处理主要包括吸附法、氧化法、生物修复法、纳米技术法和光解法[6-10],但这些方法的针对性普遍较弱,效果有限,因此,迫切需要新的、更有针对性的有效方法来消除BaA的危害。
1961年,Leman发现吖啶可以通过疏水和非共价相互作用(如π-π相互作用和范德华力)嵌入双链DNA的碱基对中[11]。从那时起,一些DNA嵌入化合物被发现具有类似的嵌入双链DNA碱基对的能力,并且可以根据它们与DNA的嵌入结合被DNA从污染物中选择性地去除。最近,一些平面多环有毒化合物,如黄曲霉毒素[12-15]、多环芳烃[16,17]和溴化乙锭(EB)[18],通过与DNA的嵌入结合,成功地被DNA选择性地吸附和去除。此外,另一项初步研究工作还表明,DNA作为一种新型的选择性吸附剂,可以有效地从水溶液中吸附BaA[19]。而且,染色质是由DNA和蛋白质组成的超级生物大分子,也拥有DNA本身。然而,目前关于染色质在吸附材料领域应用的研究还十分缺乏。通常,染色质是分离和纯化DNA的原料,DNA广泛存在于雄性鱼类、家禽和牲畜的睾丸中。因此,染色质的来源更广,比游离DNA更便宜。事实上,我们的初步研究工作表明,普通鲤鱼精子染色质确实可以有效地从污染物中去除EB[20,21]和苯并芘[22]。然而,由于染色质是一种水溶性生物大分子,处理后难以分离,这极大地限制了其应用性能。因此,迫切需要新的方法来固定染色质,以消除BaA的危害。
近年来,水凝胶因其无毒、可生物降解、可再生和吸附性强等优点,在废水处理中得到了广泛应用。水凝胶是一种由水分子和亲水性聚合物组成的凝胶系统,具有三维网络结构,可以膨胀但不溶于水[23]。它分为两类:合成水凝胶和天然聚合物水凝胶。其中,天然聚合物水凝胶因其来源广泛、价格低廉而得到广泛应用[24]。壳聚糖、海藻酸钠、丝素蛋白、卡拉胶和纤维素是最常见的天然凝胶聚合物。卡拉胶又叫鹿角菜胶、角叉菜胶,是一类从海洋红藻生物中提取的阴离子多糖[25],由硫酸基化或非硫酸基化的半乳糖与3,6-脱水半乳糖之间通过α-1,3-糖苷键与β-1,4-糖苷键交替连接,得到的一种硫酸线性半乳聚糖[26]。卡拉胶因其特有的乳化性、凝胶性、增稠性、成膜性常被用作胶凝剂、乳化剂、增稠剂和悬浮剂,广泛应用于果冻制品、软糖制品、肉制品和面制品当中,在食品加工业中发挥着重要的作用。
因此,为了解决染色质的水溶性问题并扩大其应用范围,本研究制备了一种染色质/卡拉胶复合材料,用于有效地从水溶液中吸附BaA。我们试图用荧光显微镜、傅里叶红外光谱(FTIR)、X射线衍射分析仪(XRD)和热重分析仪(TGA)分析和揭示BaA处理前后染色质/卡拉胶复合材料的结构特征。同时,我们还将研究反应时间、反应温度、pH值和复合材料剂量对BaA去除率的影响。最后,我们将使用动力学和热力学模型分析染色质/卡拉胶复合材料吸附BaA的过程。
2 实验仪器与试剂
2.1 实验仪器
BaA的浓度用Cary Eclipse荧光分光光度计(美国)测定。为了控制温度,使用中国制造的HH-4型恒温水浴锅。使用DM4B荧光显微镜(德国)观察BaA吸附前后复合材料的荧光强度。使用alpha1-4LD+冷冻干燥机(德国)冷冻干燥复合材料。美国Thermo Scientific Nicolet 10 FTIR光谱仪用于分析BaA吸附前后复合材料红外特征峰变化情况。D8A-A25 XRD用于分析复合材料的晶体结构。TG209F3 TGA(德国)用于分析染色质的热稳定性。
2.2 实验试剂
BaA(≥98%)由美国Sigma化学有限公司生产;鲤鱼睾丸购自当地养殖场;卡拉胶从合肥千盛生物科技有限公司购买。将BaA溶解在乙醇中后,用Tris-HCl缓冲液(pH 7.4)进行稀释。乙醇(98%)由成都科隆化工有限公司生产;Tris由上海源叶生物科技有限公司生产;盐酸由西陇科技有限公司制造;染色质提取试剂从西陇科技有限公司购买。本实验中所用其他试剂均为分析纯,溶液均使用三级蒸馏水配制。
3 实验方法
3.1 染色质的提取
染色质的提取是按照Artman[27]提出的方法进行的。用1.5%柠檬酸三钠溶液在16000rpm的打浆机中以1∶10(w/w)的比例匀浆10min,然后12000rpm离心15min,弃去上清液,保留沉淀。将沉淀与0.25M蔗糖-1.5%柠檬酸三钠溶液以1∶10(w/w)的比例在16000rpm的打浆机中匀浆2min,然后以1∶30(w/w)的比例倒入0.88M葡萄糖-1.5%柠檬酸三钠溶液中均匀分散10min,得到普通鲤鱼精子细胞。将匀浆液在12000rpm下离心15min,然后用0.05M Tris-HCl-0.15M氯化钠(pH 7.5)溶液按1∶5(w/w)的比例洗涤3次,得到纯细胞核精液。随后,用0.01M Tris-HCl(pH 8.0)以1∶10(w/w)的比例在16000rpm下进行均质,进一步打破细胞核。最后,将破碎的细胞核溶液以12000rpm离心15min,然后进行冷冻干燥,得到普通鲤鱼精子染色质,于4℃冰箱保存。
3.2 染色质/卡拉胶复合材料的制备
称取3g卡拉胶溶于100ml超纯水中,在90℃水浴锅中加热搅拌直至其全部溶解。量取一定体积含量为20%的染色质与卡拉胶水溶胶以1∶2(v/v)混合,搅拌5min,使二者混合均匀,然后倒入玻璃板中在室温下静置凝胶。最后将凝胶放入超低温冰箱以及冷冻干燥机中冷冻干燥48h,得到染色质/卡拉胶复合凝胶材料,于4℃冰箱中保存备用。
3.3 吸附实验
在35℃恒温水浴条件下对4mL BaA工作液进行吸附实验。使初始浓度不同的BaA溶液(0.1、0.13、0.16、0.19和0.22mg·L-1)研究了反应时间(10、30、50、70、90、120和150min)对BaA吸附率的影响。随后,还研究了温度(5、35和45℃)、pH值(5.4~9.4)和染色质/卡拉胶复合材料剂量(0.03、0.04、0.05、0.06 g)对BaA吸附率的影响。最后,收集上述所有样品的上清液,并分别用荧光分光光度计测量其荧光强度。BaA的吸附率(R,%)和吸附量(q,mg·g-1)分别表示为方程(1)和(2)。
BaA(R)=![]() ×100%(1)
×100%(1)
BaA![]() =
=![]() (2)
(2)
式中:C0是BaA溶液的初始浓度(mg·L-1);Cf是BaA溶液的剩余浓度(mg·L-1);V是BaA工作液的体积(L);W是染色质的质量(g)。
3.4 复合材料的表征
为了探索染色质/卡拉胶复合材料吸附前后的结构特征,取适量样品剪切并研磨。然后,分别对复合材料进行XRD分析、荧光显微镜观察、FTIR分析和TGA测试。
4 结果与讨论
4.1 吸附特性
4.1.1 荧光显微镜观察结果分析
从图1中可以发现,游离DNA在荧光显微镜下不会发出荧光,因为游离DNA在吸收紫外线后也不会发出荧光[如图1(a)所示]。而游离的EB作为一种典型的DNA插层剂和DNA染料,虽然在紫外线照射下也能发出非常微弱的特征荧光,但只有在插入双链DNA的碱基对后,EB才会在紫外线照射下发出强烈的荧光[28]。图1(c)的结果表明,EB确实插层到了双链DNA的碱基对中,因为与EB相互作用后的DNA在荧光显微镜下显示出强烈的荧光。与EB相似,BaA也能插层到双链DNA的碱基对中,因为与BaA反应后的DNA在荧光显微镜下也能发出强烈的荧光[如图1(d)所示]。由于染色质中除了DNA以外还含有蛋白质,然而,在蛋白质中,还含有一些自然发光的氨基酸,如色氨酸,酪氨酸和苯丙氨酸[29],因此游离染色质在荧光显微镜下也能产生一定强度的荧光[如图1(b)所示]。在荧光显微镜下可以发现,与BaA相互作用的染色质的荧光强度进一步增强,表明BaA确实插入到染色质中的双链DNA的碱基对中,从而产生了更强的荧光,与游离染色质原有的荧光颜色有明显的不同[如图1(e)所示]。图1(f)、(g)和(h)中的结果表明,卡拉胶凝胶、与BaA相互作用后的卡拉胶凝胶以及染色质/卡拉胶复合材料由于缺乏BaA与DNA之间的插层作用而不能发出强烈荧光。然而,与BaA相互作用后的染色质/卡拉胶复合材料在荧光显微镜下发出了强烈的荧光,这表明BaA确实插层到了复合材料中的染色质双链DNA的碱基对中,从而产生了更强的荧光,且与复合材料和游离染色质的原始荧光颜色有明显不同[如图1(i)所示]。这些结果表明,与DNA和染色质相似,染色质/卡拉胶复合材料也可以作为一种基于DNA嵌插结合的新型候选吸附剂选择性地从污染物中去除BaA。
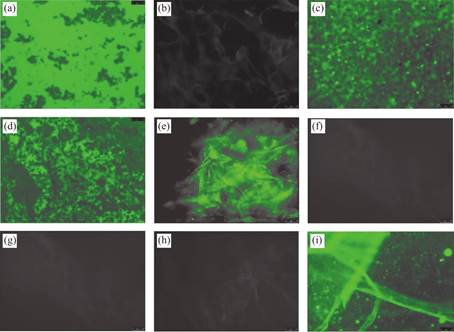
图1 荧光显微镜观察:(a)DNA的荧光显微镜图像[30],(b)染色质的荧光显微镜图像,(c)DNA吸附EB后的荧光显微镜图像,(d)DNA吸附BaA后的荧光显微镜图像[30],(e)染色质吸附BaA后的荧光显微镜图像,(f)卡拉胶凝胶的荧光显微图像,(g)卡拉胶凝胶吸附BaA后的荧光显微图像,(h)染色质/卡拉胶复合材料的荧光显微图像和(i)染色质/卡拉胶复合材料吸附BaA后的荧光显微图像
Fig.1 Fluorescence microscope observation:(a)Fluorescence microscopy image of DNA [30],(b)fluorescence microscopy image of chromatin,(c)fluorescence microscopy image of DNA after adsorbing EB,(d)fluorescence microscopy image of DNA after adsorbing BaA [30],(e)fluorescence microscopy image of chromatin after adsorbing BaA, (f)fluorescence microscopy image of carrageenan gel,(g)fluorescence microscopy image of carrageenan gel after adsorbing BaA,(h)fluorescence microscopy image of chromatin/carrageenan composite materials and(i)fluorescence microscopy image of chromatin/carrageenan after adsorbing BaA
4.1.2 FTIR检测结果分析
为了更好地揭示染色质/卡拉胶复合材料的结构特征和红外吸收峰的变化情况,采用FTIR对吸附BaA前和吸附BaA后的复合材料进行检测分析,结果如图2所示。DNA的相关FTIR结果表明,在400~1300cm-1波长范围内的一些振动峰代表了DNA分子中糖、磷脂和DNA骨架的特征峰。其中,833cm-1代表糖磷脂链振动,937cm-1和966cm-1代表DNA主干标记,1055cm-1代表糖磷脂盐振动,1085cm-1代表磷酸对称伸缩振动带,1228cm-1代表磷酸位点移动峰[31-33],双链DNA独有的A-T和C-G碱基对振动峰出现在1541cm-1处[34]。此外,染色质中蛋白质羰基特有的特征峰出现在1657c![]() 。在图2曲线(a)中可以观察到染色质成分(DNA或蛋白质)的特征峰,如833cm-1、937cm-1、966cm-1、1055cm-1、1085cm-1、1228cm-1、1541cm-1和1657cm-1,表明样品(a)确实是是染色质样本。此外,相关研究表明,卡拉胶凝胶在1640cm-1处的FTIR特征峰代表酰胺I带,酰胺键C=O的拉伸振动,1260cm-1处的FTIR特征峰表明有硫酸根存在,930cm-1是C-O键的特征峰,845cm-1是C-O-SO4的特征峰。图2曲线(b)的特征峰分别为1640cm-1、1260cm-1、930cm-1、845cm-1,表明样品(b)确实为卡拉胶凝胶样本。从图2曲线(c)中可以看出,除了卡拉胶的特征峰外,样品(c)中也有染色质相关的特征峰,说明样品(c)确实是一个染色质/卡拉胶复合材料。在图2曲线(d)中,仍然可以观察到染色质成分(DNA或蛋白质)和卡拉胶的特征峰,说明样品(d)的主要成分仍然是染色质/卡拉胶复合材料。最后,由于BaA的特征峰为1476cm-1,1476cm-1的特征峰也出现在图2曲线(d)中,因此可以证实样品(d)中存在BaA,BaA确实插入到复合材料中染色质的双链DNA碱基对中。此外,还可以证实由于复合材料中插入了BaA,染色质的特征峰1541cm-1改为1550cm-1,1085cm-1改为1072cm-1,1055cm-1改为1035cm-1,卡拉胶的特征峰1260cm-1改为1265cm-1。
。在图2曲线(a)中可以观察到染色质成分(DNA或蛋白质)的特征峰,如833cm-1、937cm-1、966cm-1、1055cm-1、1085cm-1、1228cm-1、1541cm-1和1657cm-1,表明样品(a)确实是是染色质样本。此外,相关研究表明,卡拉胶凝胶在1640cm-1处的FTIR特征峰代表酰胺I带,酰胺键C=O的拉伸振动,1260cm-1处的FTIR特征峰表明有硫酸根存在,930cm-1是C-O键的特征峰,845cm-1是C-O-SO4的特征峰。图2曲线(b)的特征峰分别为1640cm-1、1260cm-1、930cm-1、845cm-1,表明样品(b)确实为卡拉胶凝胶样本。从图2曲线(c)中可以看出,除了卡拉胶的特征峰外,样品(c)中也有染色质相关的特征峰,说明样品(c)确实是一个染色质/卡拉胶复合材料。在图2曲线(d)中,仍然可以观察到染色质成分(DNA或蛋白质)和卡拉胶的特征峰,说明样品(d)的主要成分仍然是染色质/卡拉胶复合材料。最后,由于BaA的特征峰为1476cm-1,1476cm-1的特征峰也出现在图2曲线(d)中,因此可以证实样品(d)中存在BaA,BaA确实插入到复合材料中染色质的双链DNA碱基对中。此外,还可以证实由于复合材料中插入了BaA,染色质的特征峰1541cm-1改为1550cm-1,1085cm-1改为1072cm-1,1055cm-1改为1035cm-1,卡拉胶的特征峰1260cm-1改为1265cm-1。
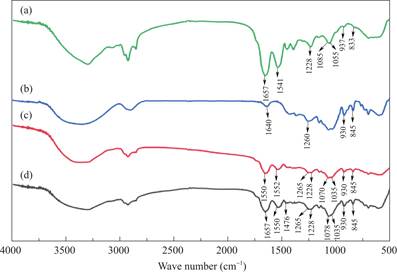
图2 (a)染色质的FTIR图,(b)卡拉胶凝胶的FTIR图,(c)染色质/卡拉胶复合材料的FTIR图和(d)染色质/卡拉胶复合材料吸附BaA后的FTIR图
Fig.2 (a)FTIR diagram of chromatin,(b)FTIR diagram of carrageenan gel,(c)FTIR diagram of chromatin/carrageenan composite materials and(d)FTIR diagram of chromatin/carrageenan composite materials after adsorbing BaA
4.1.3 XRD检测结果分析
相关研究表明,纯卡拉胶在2θ=28°、40°、50°处显示出强而尖锐的衍射峰,表明其存在长距离排列的晶体峰[35]。如图3所示,染色质的主衍射峰出现在2θ=12°,与纯卡拉胶的主衍射峰相比,染色质/卡拉胶复合材料的主衍射峰位于2θ=12°、28°、40°、50°,表明复合凝胶内部卡拉胶与染色质之间具有良好的相容性,对凝胶形成后的分子微观结构存在协同作用,进一步证实了染色质与卡拉胶形成了有效结合。
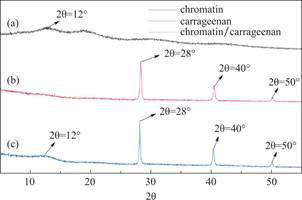
图3 染色质、卡拉胶和染色质/卡拉胶复合材料的XRD图谱
Fig.3 XRD spectra of chromatin,carrageenan and chromatin/carrageenan composite materials
4.1.4 TGA检测结果分析
由于TGA是检测物质热稳定性最重要的技术方法[36],因此我们使用TGA研究了染色质、卡拉胶凝胶和染色质/卡拉胶复合材料的热稳定性,结果如图4所示。对于染色质,我们观察到了两次重量变化。第一次重量变化发生在50~130℃,是水分损失的结果;第二次重量变化发生在200~510℃,可能是由于样品中蛋白质的分解和分子间氢键的降解造成的[37]。对于卡拉胶凝胶,观察到三次重量变化。第一次重量变化发生在50~160℃,是水分损失的结果;第二次重量变化发生在180~210℃时,是卡拉胶遇热发生剧烈分解,卡拉胶中糖苷键发生断裂及样品存在挥发[38];第三次重量变化发生在250~500℃,可能是卡拉胶热降解的副产物。而染色质/卡拉胶复合材料也出现了三次变化。第一次重量变化发生在50~200℃,是水分损失的结果;第二次重量变化发生在230~250℃,是染色质和卡拉胶热降解的结果;第三次重量变化发生在300~500℃,可能是染色质和卡拉胶热降解副产物的结果[20]。因此,染色质的加入确实可以影复合材料的热稳定性。
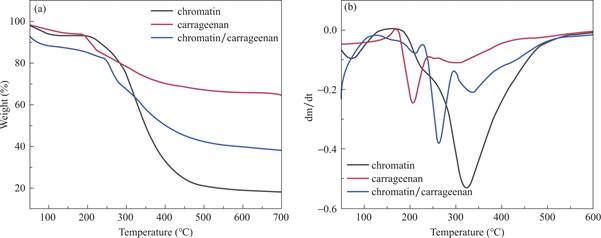
图4 复合材料的热稳定性:(a)染色质、卡拉胶、染色质/卡拉胶复合材料的TGA图和(b)染色质、卡拉胶、染色质/卡拉胶复合材料的DTG图
Fig.4 Composite materials thermal stability:(a)TGA image of chromatin,carrageenan,chromatin/carrageenan composite materials and(b)DTG image of chromatin,carrageenan,chromatin/carrageenan composite materials
4.2 染色质/卡拉胶复合材料去除BaA的影响因素探究
4.2.1 反应时间对BaA去除率的影响
反应时间是吸附过程中的一个重要影响因素,适当的反应时间能有效提高复合材料吸附剂对BaA的去除率。从图5中可以看出,吸附率随着反应时间的延长而先增大后趋于稳定。当反应时间从10min逐渐延长到120min时,每两个相邻时间的吸附率都在以较小幅度增加,当反应时间继续延长至150min时,吸附率逐渐趋于平稳,出现这一现象的原因可能是当复合材料剂量一定时,吸附剂所能提供的吸附位点数目有限。在反应发生初期,复合材料上有足够的吸附位点与BaA分子快速结合,以去除溶液中的BaA。结果表明,随着反应时间的增加,材料表面的吸附位点数量越来越少,不利于反应继续进行,吸附率逐渐趋于稳定。因此,120min是该吸附过程的最佳反应时间。
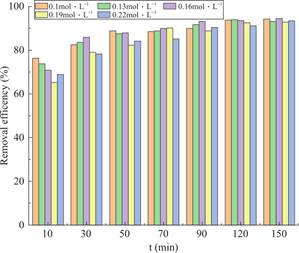
图5 反应时间对BaA去除率的影响
Fig.5 Effect of reaction time on BaA removal efficiency
4.2.2 反应温度对BaA去除率的影响
为了研究反应温度对吸附率的影响,在pH 7.4条件下建立了一系列温度梯度实验,结果如图6所示。当温度从5℃升高到35℃时,在所有浓度下,染色质/卡拉胶复合材料对BaA的吸附率都逐渐升高;当温度从35℃升高到45℃时,去除率增幅较小或略有下降,这表明该吸附过程受到温度的影响。当温度较低时,体系中的分子活性受到抑制,复合材料中的染色质与BaA分子结合率降低,然而随着温度的升高,体系中的分子活性增强,活性位点扩大,更容易发生结合,从而提高了去除率[39]。当温度高于35℃时,DNA双螺旋碱基对之间的氢键会被破坏,发生断裂并部分解旋,减少了碱基对的夹层数量,即结合位点的数量,从而影响了复合材料中BaA与染色质DNA的相互作用[30]。因此,BaA与复合材料中染色质结合的最佳反应温度为35℃。
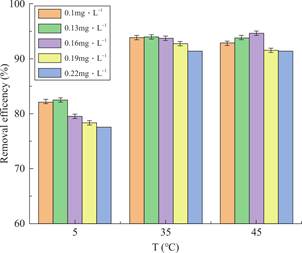
图6 温度对BaA去除效果的影响
Fig.6 Effect of temperature on BaA removal efficiency
4.2.3 染色质/卡拉胶复合材料剂量对BaA去除率的影响
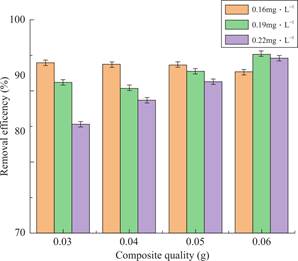
图7 复合材料剂量对BaA去除效果的影响
Fig.7 Effect of composite materials dosage on BaA removal efficiency
染色质/卡拉胶复合材料的用量直接影响对BaA的去除率。从图7可以看出,当染色质/卡拉胶复合材料的用量从0.03g增加到0.05g时,初始浓度为0.16mg·L-1、0.19mg·L-1和0.22mg·L-1的BaA溶液的吸附率都有所提高,这说明BaA的吸附率与染色质/卡拉胶复合材料的用量呈正相关。因为吸附剂用量的增加会导致吸附位点的增加,从而提高去除率。然而,当复合材料的用量增加到0.06g时,染色质/卡拉胶复合材料对BaA的吸附率并没有显著提高。因此,0.05g是本实验中复合材料的最佳用量。
4.2.4 pH对BaA去除率的影响
pH值的变化会直接影响溶液中H+和OH-的含量,从而影响复合材料对BaA的去除率。因此,在35℃下用不同pH值的Tris-HCl缓冲溶液进行了一系列实验,结果如图8所示。当pH值从5.4增加到7.4时,吸附率从82%上升到92%;当pH值从7.4增加到9.4时,吸附率从92%降低到87%。造成这种现象的原因可能有以下几种:首先,溶液中H+和OH-含量的变化会改变DNA中的磷酸结构,导致BaA与复合材料中DNA的相互作用减弱[40]。当溶液的pH值小于7.4时,溶液中含有大量的H+,从而导致染色质中的碱基被质子化,正电荷增加。同时,与中性pH溶液相比,DNA在酸性条件下与带正电荷的BaA之间的静电作用也会减弱[41]。因此,当BaA溶液的pH值较低时,吸附率降低,吸附容量变小。当BaA溶液pH值大于7.4时,溶液中的OH-较多,氢氧化物的存在可能会与BaA分子竞争吸附位点,从而干扰吸附剂对吸附质的吸附效果[42]。因此,本实验的最佳pH值为7.4。
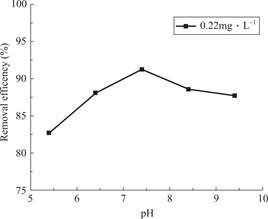
图8 pH对BaA去除效果的影响
Fig.8 Effect of pH on BaA removal efficiency
5 吸附机理研究
5.1 吸附动力学研究
吸附动力学模型可用于表征吸附剂对吸附质的去除率随时间变化的程度,从而分析整个吸附过程的方法、机理和控制机制。本实验采用准一级动力学模型和准二级动力学模型对染色质/卡拉胶复合材料吸附BaA的动力学进行了分析,两种模型分别用方程(3)和方程(4)表示[43]。
qt=qe(1-![]() )(3)
)(3)
qt=![]() (4)
(4)
式中,qe为平衡吸附量,(mg·g-1);qt为t时刻的吸附量,(mg·g-1);k1为准一级吸附动力学模型常数,(min-1);k2为准二级吸附动力学模型速率常数,g·(mg·min)-1。
准一级动力学模型、准二级动力学模型以及拟合参数分别见图9(a)、(b)和表1。可以看出准二级动力学模型得到的相关系数R2更接近1,计算得到的qe也更接近于实际测量值,因此染色质/卡拉胶复合材料对BaA的吸附过程更符合准二级动力学模型。
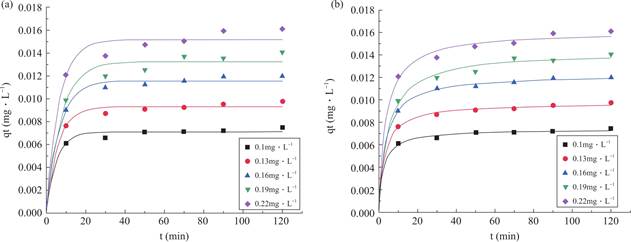
图9 (a)准一级动力学模型和(b)准二级动力学模型
Fig.9 (a)Pseudo-first-order dynamics model and(b)Pseudo-second-order dynamics model
表1 吸附动力学模型参数
Table 1 Parameters of adsorption kinetics model
|
质量浓度 (mg·g-1) |
(mg·g-1) |
准一级动力学模型 |
准二级动力学模型 |
||||
|
K1(min-1) |
qe(mg/g) |
R2 |
K2g/(mg/min) |
qe(mg/g) |
R2 |
||
|
0.1 |
0.00748 |
0.19327 |
0.0071 |
0.98874 |
58.2817 |
0.00739 |
0.996 |
|
0.13 |
0.00977 |
0.1685 |
0.00928 |
0.9895 |
34.3522 |
0.00976 |
0.998 |
|
0.16 |
0.012 |
0.14814 |
0.01158 |
0.99344 |
22.5084 |
0.01226 |
0.999 |
|
0.19 |
0.0141 |
0.12953 |
0.01326 |
0.98019 |
14.5890 |
0.01429 |
0.995 |
|
0.22 |
0.0161 |
0.15389 |
0.01517 |
0.98016 |
16.8267 |
0.01613 |
0.994 |
采用粒子内扩散模型来分析动力学结果,以阐明扩散机制[43],其表达式为方程(5)。
qt=kit0.5+C(5)
式中,Ki为粒子内扩散模型常数,mg·(g·min0.5)-1;C为与边界厚度有关的常数。
qt和t0.5的拟合结果显示了不同的线条,表明吸附过程中涉及两个或多个阶段。第一阶段相当于吸附剂的外表面吸附或瞬时吸附阶段;第二阶段被称为渐进阶段,颗粒的内部扩散调节着去除率;第三阶段为最终平衡阶段,此时因溶液中吸附质的浓度比较低,导致颗粒内部扩散开始减少[44,45]。如图10和表2所示,将qt和t0.5进行拟合,得到一条不通过原点的直线,这表明在低浓度的BaA溶液中,吸附只能在吸附剂表面进行,溶质会被完全吸附;而在高浓度的BaA溶液中,粒子内扩散并不是唯一的限速步骤。因此,BaA在染色质/卡拉胶复合材料上的吸附过程可能存在表面吸附和颗粒内扩散同时发生的两个或多个阶段。
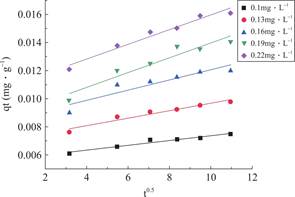
图10 粒子内扩散模型
Fig.10 Intraparticle diffusion model
表2 粒子内扩散模型参数
Table 2 Parameters of intra-particle diffusion model
|
质量浓度 (mg·L-1) |
Ki mg·(g·min0.5)-1 |
C |
R2 |
|
0.1 |
0.0001713 |
0.00565 |
0.93514 |
|
0.13 |
0.0002648 |
0.00702 |
0.93185 |
|
0.16 |
0.0003599 |
0.00845 |
0.81695 |
|
0.19 |
0.0005269 |
0.00871 |
0.89517 |
|
0.22 |
0.0005205 |
0.01074 |
0.95609 |
5.2 吸附等温线研究
吸附等温线通常采用Langmuir和Freundlich两个模型进行分析[46],以评估吸附特性、饱和吸附量和吸附剂的表面性质。Langmuir模型用方程(6)表示。
qe=![]() (6)
(6)
式中,qm是Langmuir最大单层吸附容量(mg·g-1);Ce(mg·L-1)表示吸附平衡状态下BaA的浓度;KL是Langmuir常数(L·mg-1)。
Freundlich模型用方程(7)表示。
qe=KF![]() (7)
(7)
式中,KF是Freundlich常数(mg-1-1/n·L1/n·g-1),是吸附容量的近似指标;n为吸附强度,用于衡量吸附线性偏差。
Dubinin-Radushkevich吸附等温线主要用于计算吸附过程中的平均吸附自由能E,以确定吸附过程是物理吸附还是化学吸附,用方程(8)表示。当E<8kJ·mol-1时,为物理吸附;当8KJ·moL-1<E<16KJ·moL-1时为离子交换,当E>16KJ·moL-1时为化学吸附[47]。
qe =qsexp(kadε2)(8)
式中,Kad是Dubinin-Radushkevich吸附等温线常数,(mol2·k![]() );qs为理论最大吸附量,(mg·g-1);ε为Polanyi电势,(kJ·mol-1),可用方程(9)表示。
);qs为理论最大吸附量,(mg·g-1);ε为Polanyi电势,(kJ·mol-1),可用方程(9)表示。
ε=RTln![]() (9)
(9)
式中,T为吸附时的绝对温度,(K);R为理想气体常数,8.314J·(mol·k)-1。
平均吸附自由能E(kJ·mol-1)表示从该溶液向吸附剂表面传送1mol离子所需要的自由能,可根据方程(10)计算。
E=![]() (10)
(10)
吸附等温线模型及参数如图11和表3所示,可以发现Langmuir模型的相关系数R2更接近于1,说明Langmuir模型更适合描述复合材料对BaA的吸附过程,即吸附过程可能均匀分布在吸附剂表面,染色质/卡拉胶复合材料与BaA的结合为单层吸附[48]。Freundlich模型计算出的n大于1,表明BaA与复合材料之间存在良好而强烈的相互作用。而Dubinin-Radushkevich模型得到的平均吸附自由能E<8 KJ·moL-1,因此染色质/卡拉胶复合材料对BaA的吸附属于物理吸附。总之,染色质/卡拉胶复合材料是一种高效的吸附剂,可用于去除污染物中的BaA。
5.3 吸附热力学研究
为了进一步探讨BaA与染色质/卡拉胶复合材料之间的吸附热力学特性,研究了不同温度条件下的吸附实验。吉布斯自由能(ΔG)、标准熵变(ΔS)和标准焓变(ΔH)分别用方程(11)~(14)表示[49]。
ΔG=-RTlnKd(11)
Kd=![]() (12)
(12)
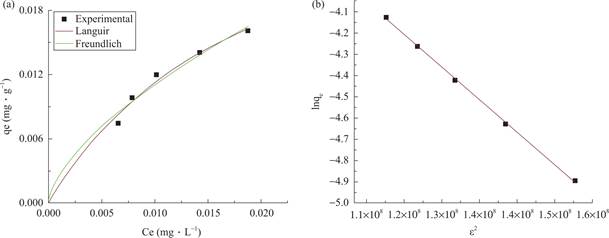
图11 (a)吸附等温线模型和(b)Dubinin-Radushkevich等温线模型
Fig.11 (a)adsorption isotherm model and(b)Dubinin-Radushkevich isotherm model
表3 吸附等温线模型参数
Table 3 Parameters of adsorption isotherm model
|
吸附等温线模型 |
R2 |
KL(L·mg-1) KF(mg-1-1/n·L1/n·g-1) Kad(mol2·kJ-2) |
n |
qm(mg·g-1) |
E(kJ·mol-1) |
|
Langmuir |
0.99065 |
49.88394 |
|
0.03377 |
|
|
Freundlich |
0.9853 |
0.20512 |
1.57756 |
|
|
|
Dubinin-Radushkevich |
0.9991 |
-1.7×10-8 |
|
|
5.423 |
ΔG=ΔH-TΔS(13)
lnKd=![]() -
-![]() (14)
(14)
式中,T为吸附温度,(K);R为气体常数,8.314J·(mol·K)-1。
热力学研究可以确定吸附剂对吸附质的吸附过程能否自发进行,结果如图12和表4所示。ΔG在所有温度下都小于0,表明染色质/卡拉胶复合材料对BaA的吸附属于自发反应。
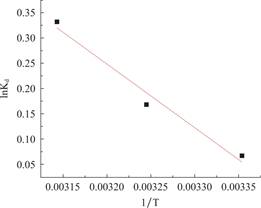
图12 吸附热力学模型
Fig.12 Adsorption thermodynamic model
表4 吸附热力学模型参数
Table 4 Parameters of adsorption thermodynamic model
|
T(K) |
ΔG(KJ·mol-1) |
ΔH(KJ·mol-1) |
ΔS(J·mol-1·K-1) |
|
288.15 |
-3.004 |
10.431 |
35.445 |
|
308.15 |
-3.214 |
|
|
|
318.15 |
-3.319 |
|
|
6 结论
本研究成功制备了一种染色质/卡拉胶复合材料,可以有效吸附水溶液中的BaA。荧光显微镜观察结果表明,染色质/卡拉胶复合材料可作为一种新型的基于DNA插层结合的吸附剂,有效吸附污染物中的BaA。FTIR结果表明,复合材料中的染色质与BaA形成了有效结合。XRD结果表明染色质均匀分散在卡拉胶凝胶中。TGA结果表明染色质可以影响复合材料的热稳定性。将0.05g染色质/卡拉胶复合材料加入4ml BaA工作液中,在35℃、pH值为7.4的条件下反应120min,复合材料对BaA的吸附效果达到最佳。吸附动力学结果表明,染色质/卡拉胶复合材料对BaA的吸附符合准二级动力学模型。粒子内扩散模型表明,在该吸附过程中,粒子扩散并不是唯一的限速步骤。吸附过程更符合Langmuir模型,表明染色质/卡拉胶复合材料与BaA的结合是单层吸附。Dubinin-Radushkevich模型结果表明染色质/卡拉胶复合材料对BaA的吸附属于物理吸附。热力学结果表明,该吸附过程是自发进行的。
总之,染色质/卡拉胶复合材料制备工艺简单,原料易得,高效,环境友好,能有效吸附水溶液中的BaA,在实际应用中具有广阔的发展前景。
利益冲突: 作者声明没有利益冲突。
[③] *通讯作者 Corresponding author:李军生,junshenglee63@aliyun.com
收稿日期:2025-02-26; 录用日期:2025-03-02; 发表日期:2025-03-28
基金项目:本项研究得到了国家自然科学基金项目(资助号22265003、21966008)的资助。
参考文献(References)
[1] HOSSAIN M D T, GIRASE A G, ORMOND R B. Evaluating the performance of surfactant and charcoal-based cleaning products to effectively remove PAHs from firefighter gear[J]. Frontiers in Materials, 2023, 10: 1142777.
https://doi.org/10.3389/fmats.2023.1142777.
[2] HUSSAR E, RICHARDS S, LIN Z-Q, et al. Human Health Risk Assessment of 16 Priority Polycyclic Aromatic Hydrocarbons in Soils of Chattanooga, Tennessee, USA[J]. Water Air and Soil Pollution, 2012, 223(9): 5535-5548.
https://doi.org/10.1007/s11270-012-1265-7.
[3] MA L L, MA C, SHI Z M, et al. Effects of fluoranthene on the growth, bioavailability and anti-oxidant system of Eisenia fetida during the ageing process[J]. European Journal of Soil Biology, 2012, 50: 21-27.
https://doi.org/10.1016/j.ejsobi.2011.11.005.
[4] ÖNDER K, MURAT B, ERCAN S, et al. The combined effects of polyethylene microplastics and benzoanthracene on Manila clam Ruditapes philippinarum[J]. Chemosphere, 2023, 329: 138664.
https://doi.org/10.1016/j.chemosphere.2023.138664.
[5] ZHANG J, LIN X, LIU W, et al. Effect of organic wastes on the plant-microbe remediation for removal of aged PAHs in soils[J]. Journal of Environmental Sciences, 2012, 24(8): 1476-1482.
https://doi.org/10.1016/S1001-0742(11)60951-0.
[6] ASYIKIN I N, NORHAFEZAH K, NURHIDAYAH H. Microbial Bioremediation Techniques for Polycyclic Aromatic Hydrocarbon(PAHs)-a Review[J]. Water, Air, & Soil Pollution, 2022, 233(4): 124.
https://doi.org/10.1007/s11270-022-05598-6.
[7] BORJI H, AYOUB G M, AL-HINDI M, et al. Nanotechnology to remove polychlorinated biphenyls and polycyclic aromatic hydrocarbons from water: a review[J]. Environmental Chemistry Letters, 2020, 18(3): 729-746.
https://doi.org/10.1007/s10311-020-00979-x.
[8] RAYAROTH M P, MARCHEL M, BOCZKAJ G. Advanced oxidation processes for the removal of mono and polycyclic aromatic hydrocarbons-A review[J]. Science of the Total Environment, 2023, 857: 159043.
https://doi.org/10.1016/j.scitotenv.2022.159043.
[9] SANCHES S, LEITAO C, PENETRA A, et al. Direct photolysis of polycyclic aromatic hydrocarbons in drinking water sources[J]. Journal of Hazardous Materials, 2011, 192(3): 1458-1465.
https://doi.org/10.1016/j.jhazmat.2011.06.065.
[10] XU Q, YUAN H, WANG H, et al. A Review on Modification Methods of Adsorbents for Naphthalene in Environment[J]. Catalysts, 2022, 12(4): 398.
https://doi.org/10.3390/catal12040398.
[11] LERMAN L S. Structural considerations in the interaction of DNA and acridines[J]. Journal of molecular biology, 1961, 3: 18-30.
https://doi.org/10.1016/S0022-2836(61)80004-1.
[12] HUANG G X, MA J, LI J S, et al. Study on the interaction between aflatoxin M1 and DNA and its application in the removal of aflatoxin M1[J]. Journal of Molecular Liquids, 2022, 355: 118938.
https://doi.org/10.1016/j.molliq.2022.118938.
[13] LI J S, WANG X X, FENG Z, et al. Optimization of aflatoxin B1 removal efficiency of DNA by resonance light scattering spectroscopy[J]. Spectrochimica Acta Part A: Molecular and Biomolecular Spectroscopy, 2023, 292: 122398.
https://doi.org/10.1016/j.saa.2023.122398.
[14] LI J, FENG Z, WANG J, et al. Interaction of aflatoxin G1 with free DN in vitro and possibility of its application in removing aflatoxin G1[J]. Journal of Environmental Science and Health Part B-Pesticides Food Contaminants and Agricultural Wastes, 2021, 56(10): 932-940.
https://doi.org/10.1080/03601234.2021.1979838.
[15] LI J S, WANG J, FAN J F, et al. Binding characteristics of aflatoxin B1 with free DNA in vitro[J]. Spectrochimica Acta Part a-Molecular and Biomolecular Spectroscopy, 2020, 230: 118054.
https://doi.org/10.1016/j.saa.2020.118054.
[16] MA J, HUANG G X, MO C, et al. Insights into the intercalative binding of benzo b fluoranthene with herring sperm DNA in vitro and its application[J]. Journal of Molecular Liquids, 2023, 378: 121628.
https://doi.org/10.1016/j.molliq.2023.121628.
[17] XIONG Y N, LI J S, HUANG G X, et al. Interacting mechanism of benzo(a)pyrene with free DNA in vitro [J]. International Journal of Biological Macromolecules, 2021, 167: 854-861.
https://doi.org/10.1016/j.ijbiomac.2020.11.042.
[18] ZHANG J, LI J S, HUANG G X, et al. DNA Extracted from Byproducts of Common Carp Testis and Application in Removing Ethidium Bromide from Pollutants[J]. Journal of Aquatic Food Product Technology, 2022, 31(6): 536-548.
https://doi.org/10.1080/10498850.2022.2080516.
[19] HUANG G X, MA J, LI J S, et al. Removal of 1, 2- benzanthracene via the intercalation of 1, 2-benzanthracene with DNA and magnetic bead-based separation[J]. Nucleosides Nucleotides & Nucleic Acids, 2021, 40(2): 137-156.
https://doi.org/10.1080/15257770.2020.1839905.
[20] JIANG Z K, LI J S, HUANG G X, et al. Efficient removal of ethidium bromide from aqueous solutions using chromatin-loaded chitosan polyvinyl alcohol composites[J]. Environmental science and pollution research international, 2024, 31(2): 3276-3295.
https://doi.org/10.1007/s11356-023-31364-0.
[21] ZHANG J, LI J S, HUANG G X, et al. Chromatin extracted from common carp testis as an economical and easily available adsorbent for ethidium bromide decontamination[J]. Heliyon, 2022, 8(6): e09565.
https://doi.org/10.1016/J.HELIYON.2022.E09565.
[22] JIANG Z K, LI J S, HUANG G X, et al. Common carp sperm chromatin as an economical and effective remover for benzo(a)pyrene from pollutants[J]. Heliyon, 2024, 10(12): e33137.
https://doi.org/10.1016/J.HELIYON.2024.E33137.
[23] LUNDBERG P, BRUIN A, KLIJNSTRA J W, et al. Poly( ethylene glycol)-Based Thiol-ene Hydrogel Coatings- Curing Chemistry, Aqueous Stability, and Potential Marine Antifouling Applications[J]. Acs Applied Materials & Interfaces, 2010, 2(3): 903-912.
https://doi.org/10.1021/am900875g.
[24] KAROYO A H, WILSON L D. A Review on the Design and Hydration Properties of Natural Polymer- Based Hydrogels[J]. Materials, 2021, 14(5): 1095.
https://doi.org/10.3390/ma14051095.
[25] TOLSTOGUZOV V. Some thermodynamic considerations in food formulation[J]. Food Hydrocolloids, 2003, 17(1): 1-23.
https://doi.org/10.1016/S0268-005X(01)00111-4.
[26] CAMPO V L, KAWANO D F, DA SILVA D B, JR. , et al. Carrageenans: Biological properties, chemical modifications and structural analysis-A review[J]. Carbohydrate Polymers, 2009, 77(2): 167-180.
https://doi.org/10.1016/j.carbpol.2009.01.020.
[27] ARTMAN M, ROTH J S. Chromosomal RNA: an artifact of preparation?[J]. Journal of molecular biology, 1971, 60(2): 291-301.
https://doi.org/10.1016/0022-2836(71)90295-6.
[28] LE PECQ J B, PAOLETTI C. A new fluorometric method for RNA and DNA determination[J]. Analytical biochemistry, 1966, 17(1): 100-107.
https://doi.org/10.1016/0003-2697(66)90012-1.
[29] CHENG Z, KURU E, SACHDEVA A, et al. Fluorescent amino acids as versatile building blocks for chemical biology[J]. Nature Reviews Chemistry, 2020, 4(6): 275-290.
https://doi.org/10.1038/s41570-020-0186-z.
[30] HUANG G X, LI J S, YAN L J, et al. Adsorption of 1, 2-Benzanthracene from Aqueous Solution by DNA-Conjugated Magnetic Nanoparticles[J]. Water Air & Soil Pollution, 2022, 233(1): 9.
https://doi.org/10.1007/s11270-021-05476-7.
[31] JANGIR D K, CHARAK S, MEHROTRA R, et al. FT- IR and circular dichroism spectroscopic study of interaction of 5-fluorouracil with DNA[J]. Journal of Photochemistry and Photobiology B-Biology, 2011, 105(2): 143-148.
https://doi.org/10.1016/j.jphotobiol.2011.08.003.
[32] JANGIR D K, TYAGI G, MEHROTRA R, et al. Carboplatin interaction with calf-thymus DNA: A FTIR spectroscopic approach[J]. Journal of Molecular Structure, 2010, 969(1-3): 126-129.
https://doi.org/10.1016/j.molstruc.2010.01.052.
[33] SAITO S T, SILVA G, PUNGARTNIK C, et al. Study of DNA-emodin interaction by FTIR and UV-vis spectroscopy[J]. Journal of Photochemistry and Photobiology B-Biology, 2012, 111: 59-63.
https://doi.org/10.1016/j.jphotobiol.2012.03.012.
[34] DENG Y E, ZHOU Q, SUN S Q. Analysis and discrimination of infant powdered milk via FTIR spectroscopy[J]. Guang pu xue yu guang pu fen xi = Guang pu, 2006, 26(4): 636-639.
https://doi.org/10.1016/j.sab.2006.01.014.
[35] VIEIRA W T, DA SILVA M G C, NASCIMENTO L D O, et al. k-Carrageenan/sericin-based multiparticulate systems: A novel gastro-resistant polymer matrix for indomethacin delivery[J]. International Journal of Biological Macromolecules, 2023, 232: 123381.
https://doi.org/10.1016/j.ijbiomac.2023.123381.
[36] EL MIRI N, ABDELOUAHDI K, ZAHOUILY M, et al. Bio-nanocomposite films based on cellulose nanocrystals filled polyvinyl alcohol/chitosan polymer blend[J]. Journal of Applied Polymer Science, 2015, 132(22): 39950.
https://doi.org/10.1002/app.42004.
[37] OLADIPO A, KPOMAH B, EJEROMEDOGHENE O, et al. Facile fabrication and antibacterial properties of chitosan/acrylamide/gold nanocomposite hydrogel incorporated with Chaetomium globosium extracts from Gingko biloba leaves[J]. International Journal of Biological Macromolecules, 2024, 255: 128194.
https://doi.org/10.1016/j.ijbiomac.2023.128194.
[38] 龙小菊, 王欣怡, 肖琼, 等. ι-卡拉胶低浓度碱均相提取工艺优化及其性质分析[J]. 食品工业科技, 2015: 1-15.
https://doi.org/10.13386/j.issn1002-0306.2024070413.
[39] POURETEDAL H R, SADEGH N. Effective removal of Amoxicillin, Cephalexin, Tetracycline and Penicillin G from aqueous solutions using activated carbon nanoparticles prepared from vine wood[J]. Journal of Water Process Engineering, 2014, 1: 64-73.
https://doi.org/10.1016/j.jwpe.2014.03.006.
[40] GARCIA B, LEAL J M, PAIOTTA V, et al. Intercalation of ethidium into triple-strand poly(rA). 2poly(rU): a thermodynamic and kinetic study[J]. The journal of physical chemistry B, 2006, 110(32): 16131-16138.
https://doi.org/10.1021/jp0613283.
[41] AHMADPOUR A, EFTEKHARI N, AYATI A. Performance of MWCNTs and a low-cost adsorbent for Chromium(VI)ion removal[J]. Journal of Nanostructure in Chemistry, 2014, 4(4): 171-178.
https://doi.org/10.1007/s40097-014-0119-9.
[42] FARRAG M, ABRI S, LEIPZIG N D. pH-dependent RNA isolation from cells encapsulated in chitosanbased biomaterials[J]. International Journal of Biological Macromolecules, 2020, 146: 422-430.
https://doi.org/10.1016/j.ijbiomac.2019.12.263.
[43] VENKATESHA T G, VISWANATHA R, NAYAKA Y A, et al. Kinetics and thermodynamics of reactive and vat dyes adsorption on MgO nanoparticles[J]. Chemical Engineering Journal, 2012, 198-199: 1-10.
https://doi.org/10.1016/j.cej.2012.05.071.
[44] CHIOU M-S, CHUANG G-S. Competitive adsorption of dye metanil yellow and RB15 in acid solutions on chemically cross-linked chitosan beads[J]. Chemosphere, 2006, 62(5): 731-740.
https://doi.org/10.1016/j.chemosphere.2005.04.068.
[45] HEIBATI B, YETILMEZSOY K, ZAZOULI M A, et al. Adsorption of ethidium bromide(EtBr)from aqueous solutions by natural pumice and aluminium-coated pumice[J]. Journal of Molecular Liquids, 2016, 213: 41-47.
https://doi.org/10.1016/j.molliq.2015.08.063.
[46] CHARIZANI A, NOLI F. Investigation of biosorption process of barium radionuclides on pomegranate peel; isotherms, kinetics and mechanism[J]. Journal of Radioanalytical and Nuclear Chemistry, 2022, 331(2): 807-815.
https://doi.org/10.1007/s10967-021-08152-6.
[47] TRAN H N, YOU S-J, CHAO H-P. Thermodynamic parameters of cadmium adsorption onto orange peel calculated from various methods: A comparison study[J]. Journal of Environmental Chemical Engineering, 2016, 4(3): 2671-2682
https://doi.org/10.1016/j.jece.2016.05.009.
[48] MEREY S, SINAYUC C. Gas-in-place calculations in shale gas reservoirs using experimental adsorption data with adsorption models[J]. The Canadian Journal of Chemical Engineering, 2016, 94(9): 1683-1692.
https://doi.org/10.1002/cjce.22538.
[49] MURUGESAN A, DIVAKARAN M, RAVEENDRAN P, et al. An Eco-friendly Porous Poly(imide-ether)s for the Efficient Removal of Methylene Blue: Adsorption Kinetics, Isotherm, Thermodynamics and Reuse Performances[J]. Journal of Polymers and the Environment, 2019, 27(5): 1007-1024.
https://doi.org/10.1007/s10924-019-01408-z
Characteristics and Influencing Factors of Efficient Adsorption of Benzoanthracene by Chromatin/ Carrageenan Composite Materials
(School of Biological and Chemical Engineering, Guangxi University of Science and Technology, Liuzhou 545006, China)
Abstract: Benzoanthracene (BaA) is one of the most important pollutants in polycyclic aromatic hydrocarbons ( PAHs) , with characteristics such as wide distribution, strong stability, strong bioaccumulation, and strong carcinogenicity, seriously endangering human health and the environment. In this study, a novel chromatin/carrageenan composite materials was prepared based on the intercalation binding between BaA and DNA, which is a simple and effective adsorbent that can effectively adsorb BaA from aqueous solution. Under optimal conditions, the chromatin/carrageenan composite material exhibits a BaA adsorption efficiency of 94% and an adsorption amount of 0. 0075mg·g-1. This adsorption process is influenced by reaction time, reaction temperature, pH value, and the dosage of the composite materials. Among them, high or low temperatures, acidic or alkaline environments will all reduce the adsorption efficiency. However, with the extension of reaction time or the increase of composite materials dosage, the adsorption efficiency will gradually increase. The process of removing BaA from chromatin/carrageenan composite material is more in line with pseudo-second-order kinetic model and Langmuir model, and thermodynamic model further indicated that the process is spontaneous. The above results indicate that chromatin/ carrageenan composite materials can serve as a novel adsorbent for BaA adsorption.
Keywords: Chromatin, Carrageenan, Benzoanthracene, adsorbtion
Citation: ZANG Meng, LI Junsheng, HUANG Guoxia, et al. Characteristics and influencing factors of efficient adsorption of Benzoanthracene by Chromatin/Carrageenan composite materials[J]. Acta Interdisciplinary Science, 2025, 2(1): 22-36